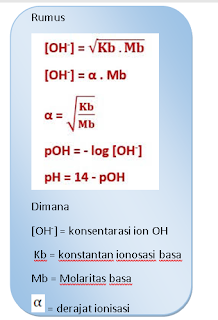
pH Larutan Asam dan Basa
1.
Asam kuat
Contoh:
HCl =asam klorida, H2SO4 = asam Sulfat,
HNO3=asam nitrat, HBr =asam bromida
HI = asam Iodida, HClO3=
asam klorat,
HClO4= asam
perklorat
2.
Basa Kuat
NaOH= Natrium Hidroksida, KOH= Kalium hidroksida,
Mg(OH)2 =
magnesium hidroksida, Ca(OH)2= calsium hidroksida,
Ba (OH)2= barium
hidroksida
3.
Asam Lemah
Contoh :
CH3COOH= asam
asetat / cuka, H2CO3=
asam karbonat,
HCN= asam sianida, HCOOH=
asam kormat,
HF= asam florida, HNO2=
asam nitrit
4.
Basa Lemah
NH4OH= amonium hidroksida, Fe(OH)2= besi II hidroksida ,
Al(OH)2= aluminium hidroksida
Contoh soal asam Kuat
Tentukan pH dari :
- 200 ml h2SO4 0,3M (log 6 = 0,8)
- 6,3 gram HNO3 dalam 200ml air (Ar H=1, N=14, O=16)
Solusi :
1.
pH = - log a x M
= - log 2 x 3.10-1
= - log 6.10-1
= 1 – log 6
= 1 – 0,8
=
0,2
2.
Mr HNO3 = 1.1 +
1.14 + 3.16
= 63
M
= gram /Mr = 6,3/63 = 0,1 = 0,5 M
Liter 0,2 0,2
pH
= - log a x Ma
= - log 1 x 5.10-1
= - log 5.10-1
= 1 – log 5
3.
Tentuan PH dari 4 gram NaOH dalam 500 ml larutan.
(Ar Na=23, O=16, H=1)
Solusi
:
Mr NaOH = 23+16+1
= 40
M = (gram/Mr)/Liter
=
(4/40)
= 0,2 M
POH
= -log b x Mb
= -log 1 x 2.10-1
=
1-log 2
PH
= 14-POH
= 14 – (1 - log 2)
= 13 + log 2
4.
Tentukan PH dari 100 ml CH3COOH 0,4 M
(Ka = 10-5)
Solusi
:
[H+] = √(Ka x Ma)
= √(10-5 x 4.10-1)
= √(4.10-6)
= 2.10-3
PH = -log
[H+]
= -log [2.10-3]
= 3 - log 2
Silahkan salin materi pada buku catatan. Lalu isi presesnsi disini: https://forms.gle/ybfKSxErtdyBvuK37
sumber .https://www.youtube.com/watch?v=01OoyRxD6A4&t=885s